Το SPRAVATO® είναι μία επαναστατική θεραπεία για την ανθεκτική στη θεραπεία κατάθλιψη (ΑΘΚ) και το πρώτο αντικαταθλιπτικό σε μορφή ρινικού εκνεφώματος*.
1 συσκευή = 28 mg
Χωρίς κλιμάκωση

Απλή αυτοχορήγηση υπό την άμεση επίβλεψη επαγγελματία υγείας
- Ένας ψεκασμός σε κάθε ρουθούνι ανά συσκευή
- Χρησιμοποιήστε 1-3 συσκευές ανάλογα με τη δόση που απαιτείται, αφήνοντας να περάσουν 5 λεπτά μεταξύ της χρήσης κάθε συσκευής

Οι ασθενείς πρέπει να παρακολουθούνται από επαγγελματία υγείας
- Οι ασθενείς θα μπορούν να αποχωρήσουν όταν είναι κλινικά σταθεροί και κρίνεται ότι μπορούν να αποχωρήσουν από τη δομή υγειονομικής περίθαλψης

Η πλειονότητα των ασθενών ήταν σε θέση να αποχωρήσουν εντός 90 λεπτών**,
- Περίπου το ήμισυ των ασθενών ήταν σε θέση να αποχωρήσουν από τη δομή εντός 1 ώρας
- Σχεδόν όλοι (93,2%) οι ασθενείς ήταν σε θέση να αποχωρήσουν από τη δομή εντός 90 λεπτών
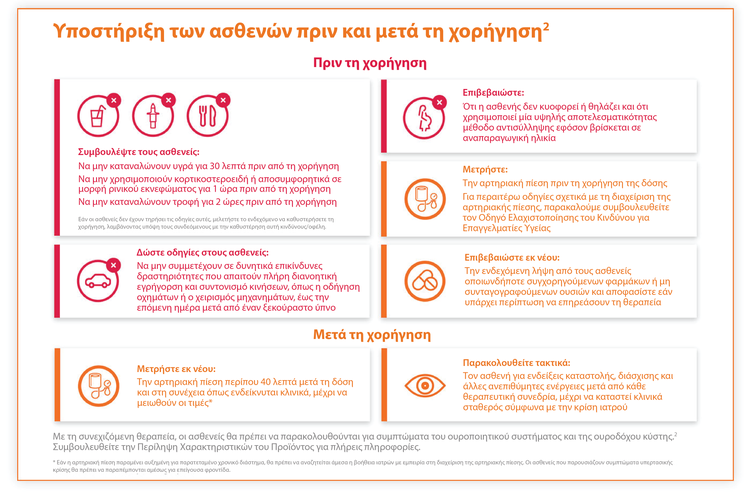
Οδηγίες για τους ασθενείς πριν και μετά τη χορήγηση
Τρόπος χορήγησης του SPRAVATO®

Σε ασθενείς των οποίων η αρτηριακή πίεση (ΑΠ) πριν από τη χορήγηση δόσης κρίνεται ότι είναι αυξημένη (ως γενική οδηγία: >140/90 mmHg για ασθενείς ηλικίας <65 ετών και >150/90 mmHg για ασθενείς ηλικίας ≥65 ετών), θα πρέπει να προσαρμόζεται ο τρόπος ζωής και/ή οι φαρμακολογικές θεραπείες προκειμένου να μειωθεί η αρτηριακή πίεση πριν από την έναρξη θεραπείας με το SPRAVATO®.
Προσαρμογή από την Περίληψη Χαρακτηριστικών Προϊόντος του SPRAVATO®. 2024.
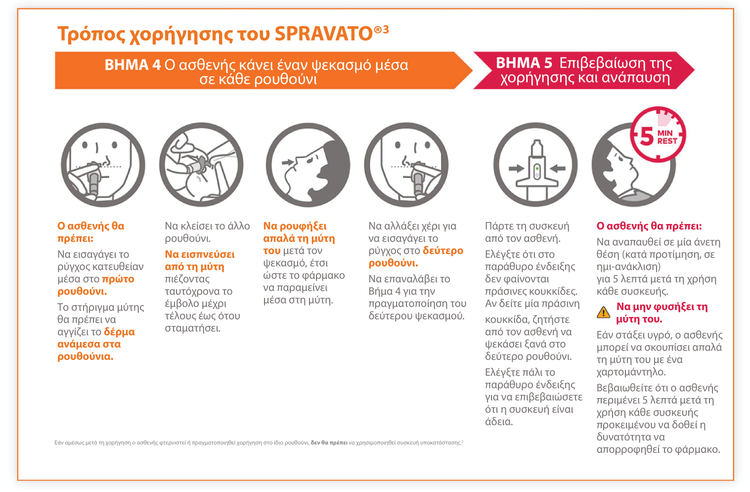
Προσαρμογή από τις Οδηγίες Χρήσης του SPRAVATO®. 2024.
Ερωτήσεις ελέγχου κατά την ολοκλήρωση της περιόδου παρακολούθησης

Τι χρειάζεται για τη χορήγηση του SPRAVATO®;

Το SPRAVATO®, σε συνδυασμό με έ�να SSRI ή SNRI, ενδείκνυται για ενήλικες με ανθεκτική στη θεραπεία Μείζονα Καταθλιπτική Διαταραχή, οι οποίοι δεν έχουν ανταποκριθεί σε τουλάχιστον δύο διαφορετικές θεραπείες με αντικαταθλιπτικά κατά το τρέχον μέτριο έως σοβαρό καταθλιπτικό επεισόδιο.
Το SPRAVATO®, συγχορηγούμενο με από στόματος χορηγούμενη αντικαταθλιπτική θεραπεία, ενδείκνυται σε ενήλικες με μέτριο έως σοβαρό επεισόδιο Μείζονος Καταθλιπτικής Διαταραχής, ως οξεία βραχυχρόνια θεραπεία, για την ταχεία μείωση των καταθλιπτικών συμπτωμάτων, τα οποία σύμφωνα με την κλινική κρίση συνιστούν ένα ψυχιατρικό επείγον περιστατικό.SPC
* Μετά την ανάπτυξη και την έγκριση του SSRI φλουοξετίνη το 1987, οι εγκεκριμένες θεραπείες (συμπεριλαμβανομένων των «άτυπων» αντικαταθλιπτι�κών όπως η μιρταζαπίνη, η αγομελατίνη κ.λπ.) συνέχισαν να στοχεύουν κυρίως το μονοαμινεργικό σύστημα. Αντιθέτως, το SPRAVATO® δρα ως ανταγωνιστής του NMDA υποδοχέα του γλουταμινικού και θεωρείται ότι οδηγεί σε διέγερση του υποδοχέα AMPAR και της νευροτροφικής σηματοδότησης.
** Ο χρόνος κατά τον οποίο οι ασθενείς ήταν σε θέση να αποχωρήσουν από τη δομή αξιολογείται σε κάθε συνεδρία θεραπείας. Οι τιμές ≥44,3% και ≥93,2% αντιπροσωπεύουν τις ημέρες κατά τις οποίες ήταν σε θέση να αποχωρήσει το χαμηλότερο ποσοστό ασθενών στα αντίστοιχα χρονικά σημεία.
Συντομογραφίες
ΑΘΚ: ανθεκτική στη θεραπεία κατάθλιψη, ΑΚ: αντικαταθλιπτικό, AMPAR: υποδοχέας α-αμινο-3-υδροξυ-5-μεθυλ-4-ισοξαζολοπροπιονικού οξέος, ΑΠ: αρτηριακή πίεση, ΜΚΔ: μείζων καταθλιπτική διαταραχή, NMDA: N-μεθυλ-D-ασπαρτικό, SSRI: εκλεκτικός αναστολέας επαναπρόσληψης σεροτονίνης.

Με ειδική ιατρική συνταγή του Ν3459/06 περί ναρκωτικών (Πίνακας Γ): Μόνο για Νοσοκομειακή χρήση.
ΡΙΝΙΚΟ ΕΚΝΕΦΩΜΑ, ΔΙΑΛΥΜΑ 28ΜΓ/περιέκτη (VIAL) - 1 περιέκτης εκνεφώματος (VIAL): N.T. 167,59 €, Λ.Τ. 232,79 €
.png)